- ปี พ.ศ.2549 กรมควบคุมโรค ได้มีคำสั่งแต่งตั้งคณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค ทำหน้าที่พิจารณาให้ความเห็นชอบเชิงจริยธรรมแก่โครงการวิจัย เพื่อให้การดำเนินงานวิจัยที่เกี่ยวข้องกับมนุษย์ เป็นไปตามหลักสากลและสอดคล้องตามหลักจริยธรรมการวิจัยในคน อันเป็นหลักประกันการคุ้มครองศักดิ์ศรี สิทธิ ความปลอดภัย และความเป็นอยู่ที่ดีของอาสาสมัคร
- ปี พ.ศ. 2565 ได้มีคำสั่งแต่งตั้ง คณะกรรมการจริยธรรมการวิจัยที่ไม่ได้ดำเนินการในมนุษย์ กรมควบคุมโรค โดยมี นายแพทย์สมเกียรติ ศิริรัตนพฤกษ์ เป็นประธาน เนื่องจากในการดำเนินงาน ที่ผ่านมาการติดตามการดำเนินงานของโครงการวิจัยที่ไม่ได้ดำเนินการในมนุษย์ยังไม่มีระบบการดำเนินงาน ที่ชัดเจน ทำให้ภายหลังจากที่โครงการวิจัยได้รับการอนุมัติรับรองไปแล้ว ไม่มีกระบวนการในการติดตามการดำเนินงาน
ปัจจุบัน นายแพทย์ศุภชัย ฤกษ์งาม เป็นประธานคณะกรรมการ มีกรรมการจำนวนทั้งสิ้น 17 คน ประกอบด้วยผู้ทรงคุณวุฒิที่มีความรู้ ความเชี่ยวชาญและประสบการณ์หลายสาขา ทั้งภายนอกและภายในกรมควบคุมโรค ตามคำสั่งกรมควบคุมโรคที่ 19/2566 สั่ง ณ วันที่ 3 มกราคม พ.ศ. 2566 คณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค ได้ดำเนินการลงทะเบียนในระบบของ Office for Human Research Protection: OHRP ประเทศสหรัฐอเมริกา โดยปฏิบัติตามแนวทาง The Declaration of Helsinki / The Belmont Report / CIOMS / ICH-GCP เลขทะเบียน FWA 00013622 (Expire 08/06/2028) และ IRB 00006655 (Expire 19/02/2024) มาตรฐานการดำเนินงาน (Standard Operating Procedures) ของคณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค ฉบับแก้ไขครั้งที่ 1 เมื่อ มกราคม 2562
การศึกษาวิจัยที่มีบุคลากรกรมควบคุมโรคเป็นผู้วิจัยหลัก, ผู้วิจัยร่วม และ/หรือใช้สถานที่ อุปกรณ์ งบประมาณ หรือสิ่งอำนวยความสะดวกของกรมควบคุมโรค ต้องส่งโครงร่างการวิจัยเพื่อขอรับรองด้านจริยธรรมการวิจัยจากคณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค คณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค จะไม่รับพิจารณาโครงร่างวิจัยที่เริ่มดำเนินการก่อนได้รับการรับรองจากคณะกรรมการฯ ผู้วิจัยสามารถศึกษาจากคู่มือ คำแนะนำในการจัดทำและจัดส่งโครงการวิจัยเพื่อรับการพิจารณาจากคณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค (ฉบับปรับปรุงครั้งที่ 3 เมษายน พ.ศ.2555)
คณะกรรมการฯ จะพิจารณาโครงร่างการวิจัยทุกวันอังคารที่ 2 ของทุกเดือน หากมีโครงร่างการวิจัยจำนวนมากอาจพิจารณาประชุมเพิ่มเติมในวันอังคารที่ 4 ของเดือน ทั้งนี้ ขอให้ผู้วิจัยส่งโครงร่างการวิจัยพร้อมบันทึกนำส่งจากหน่วยงานหรือผู้วิจัย เรียน ประธานคณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค ส่งถึงฝ่ายเลขานุการคณะกรรมการฯ ตามกำหนดวันรับโครงการ
ตารางการประชุมประจำปีงบประมาณ พ.ศ.2567
กำหนดวันประชุมอย่างน้อยเดือนละ 1 ครั้ง
ตารางการประชุมประจำปีงบประมาณ พ.ศ.2567
กำหนดวันประชุมอย่างน้อยเดือนละ 1 ครั้ง
ปี พ.ศ. 2565 ได้มีคำสั่งแต่งตั้ง คณะกรรมการจริยธรรมการวิจัยที่ไม่ได้ดำเนินการในมนุษย์ กรมควบคุมโรค โดยมี นายแพทย์สมเกียรติ ศิริรัตนพฤกษ์ เป็นประธาน เนื่องจากในการดำเนินงาน ที่ผ่านมาการติดตามการดำเนินงานของโครงการวิจัยที่ไม่ได้ดำเนินการในมนุษย์ยังไม่มีระบบการดำเนินงาน ที่ชัดเจน ทำให้ภายหลังจากที่โครงการวิจัยได้รับการอนุมัติรับรองไปแล้ว ไม่มีกระบวนการในการติดตาม การดำเนินงาน เช่น การเปลี่ยนแปลงโครงการวิจัย การยุติโครงการหากไม่ได้มาตรฐานการดำเนินงาน ดังนั้น จึงได้มีการจัดตั้งคณะกรรมการฯ ชุดนี้ เพื่ออนุมัติรับรองโครงร่างการวิจัยที่ไม่เกี่ยวข้องกับมนุษย์ ของบุคลากรภายใน กรมควบคุมโรค คณะกรรมการฯ จะพิจารณาโครงร่างการวิจัยทุกวันวันจันทร์ที่ 2 ของทุกเดือน หากไม่มีโครงร่างวิจัยเข้ามาจะเลื่อนประชุมออกไปเป็นวันจันทร์ที่ 2 ของเดือนถัดไป ทั้งนี้ ขอให้ผู้วิจัยส่งโครงร่างการวิจัยพร้อมบันทึกนำส่งจากหน่วยงานหรือผู้วิจัย เรียน ประธานคณะกรรมการจริยธรรมการวิจัยที่ไม่ได้ดำเนินการในมนุษย์ กรมควบคุมโรค ส่งถึงฝ่ายเลขานุการคณะกรรมการฯ
ภาพกระบวนการ
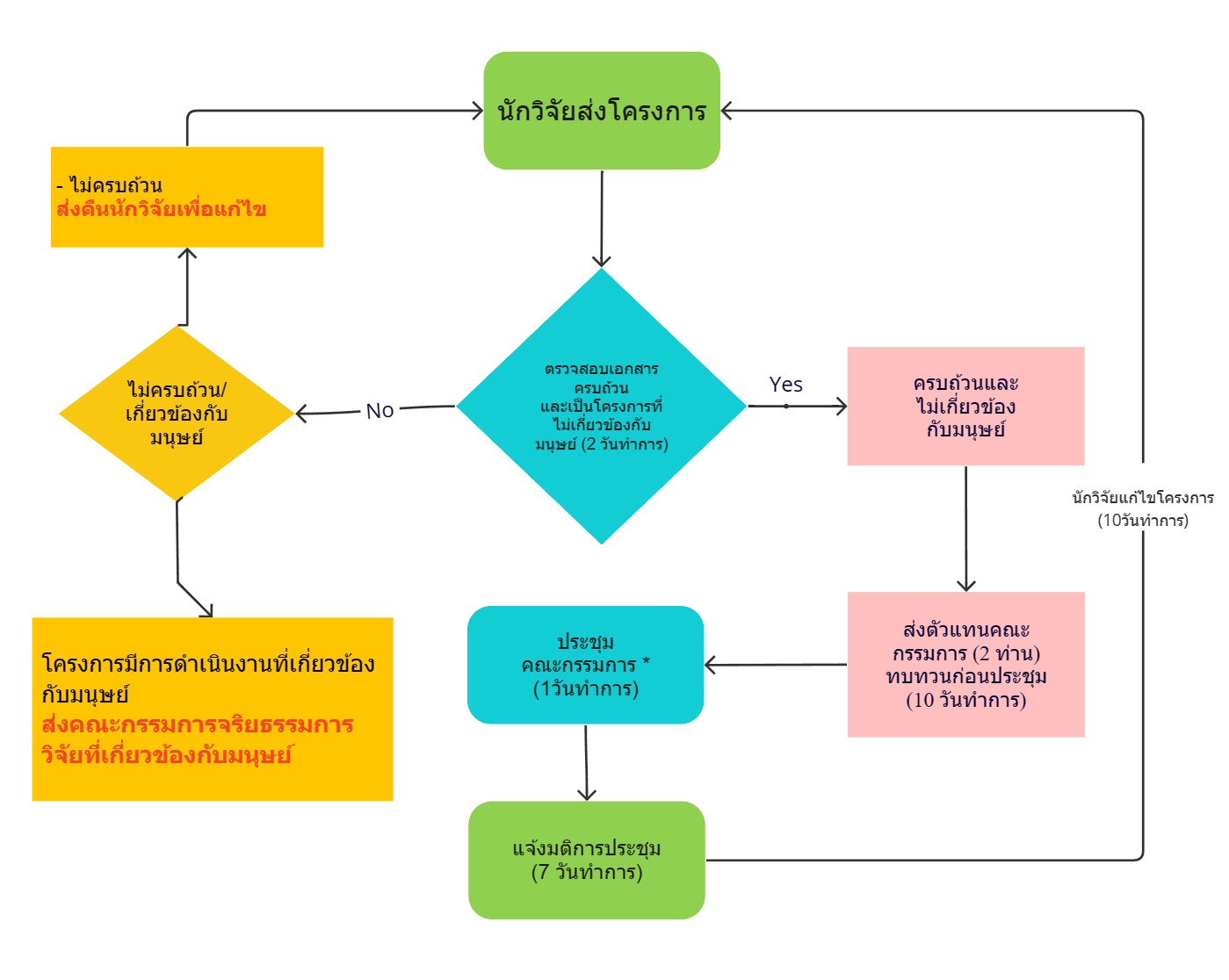
ภาพกระบวนการ

การวิจัยที่เกี่ยวข้องกับมนุษย์ (จำนวน 13 ชุด)
- 1.1 แบบตรวจสอบความครบถ้วนของ หัวข้อต่างๆ ในแบบเสนอโครงการวิจัย 1 ชุด
- 1.2 แบบเสนอโครงการวิจัย**ไม่ต้องเข้ารูปเล่ม**
- 1.3 เอกสารแนะนำสำหรับอาสาสมัครและใบยินยอมเข้าร่วมโครงการของอาสาสมัคร **จำนวนเอกสารต้องส่งตามจำนวนโครงร่างวิจัย**
- ♦ information sheet
- ♦ consent form
- ♦ information sheet 7-12 years
- ♦ consent form 7-12 years
- ♦ consent form parents & legally authorized representative (LAR)
- 1.4 กรณีที่ผู้วิจัยได้รับมติให้ปรับปรุงแก้ไขโครงร่างการวิจัย กรุณาส่งแบบสรุปประเด็นที่แก้ไขตามมติกรรมการ
- 1.1 แบบตรวจสอบความครบถ้วนของ หัวข้อต่างๆ ในแบบเสนอโครงการวิจัย 1 ชุด
- 1.2 แบบเสนอโครงการวิจัย**ไม่ต้องเข้ารูปเล่ม**
- 1.3 เอกสารแนะนำสำหรับอาสาสมัครและใบยินยอมเข้าร่วมโครงการของอาสาสมัคร **จำนวนเอกสารต้องส่งตามจำนวนโครงร่างวิจัย**
- ♦ information sheet
- ♦ consent form
- ♦ information sheet 7-12 years
- ♦ consent form 7-12 years
- ♦ consent form parents & legally authorized representative (LAR)
- 1.4 กรณีที่ผู้วิจัยได้รับมติให้ปรับปรุงแก้ไขโครงร่างการวิจัย กรุณาส่งแบบสรุปประเด็นที่แก้ไขตามมติกรรมการ
- ♦ แบบเสนอขอแก้ไขในโครงร่างการวิจัย (Protocol Amendment)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ โครงร่างวิจัยที่มีการเปลี่ยนแปลง (ทำ Highlight ส่วนที่มีการแก้ไข) 2.2 การรายงานไม่ปฏิบัติตามโครงร่างการวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการไม่ปฏิบัติตามโครงร่างการวิจัยที่ได้รับรอง (Protocal non - compliance Report) 2.3 รายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report) 2.4 การขอต่ออายุโครงร่างวิจัย/ ขยายเวลาโครงร่างวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานความก้าวหน้าของการวิจัย 2.5 การแจ้งยุติโครงการวิจัยก่อนกำหนด
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการยุติโครงการวิจัยก่อนกำหนด (Premature termination) 2.6 การแจ้งปิดโครงการวิจัย (เมื่อดำเนินการวิเคราะห์ข้อมูลเสร็จสิ้น)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเสร็จสิ้นโครงการวิจัย(Final Report)
- ♦ แบบเสนอขอแก้ไขในโครงร่างการวิจัย (Protocol Amendment)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ โครงร่างวิจัยที่มีการเปลี่ยนแปลง (ทำ Highlight ส่วนที่มีการแก้ไข) 2.2 การรายงานไม่ปฏิบัติตามโครงร่างการวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการไม่ปฏิบัติตามโครงร่างการวิจัยที่ได้รับรอง (Protocal non - compliance Report) 2.3 รายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเหตุการณ์ไม่พึงประสงค์จากการวิจัย (Adverse Event Report) 2.4 การขอต่ออายุโครงร่างวิจัย/ ขยายเวลาโครงร่างวิจัย
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานความก้าวหน้าของการวิจัย 2.5 การแจ้งยุติโครงการวิจัยก่อนกำหนด
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานการยุติโครงการวิจัยก่อนกำหนด (Premature termination) 2.6 การแจ้งปิดโครงการวิจัย (เมื่อดำเนินการวิเคราะห์ข้อมูลเสร็จสิ้น)
- ♦ สำเนาโครงร่างวิจัยที่ได้รับการรับรองฉบับล่าสุด
- ♦ แบบรายงานเสร็จสิ้นโครงการวิจัย (Final Report)
กรณี อาสาสมัครอายุ 18 ปีขึ้นไป
กรณี อาสาสมัครอายุต่ำกว่า 18 ปี
การวิจัยที่ไม่เกี่ยวข้องกับมนุษย์ (จำนวน 10 ชุด)
กรณี อาสาสมัครอายุ 18 ปีขึ้นไป
กรณี อาสาสมัครอายุต่ำกว่า 18 ปี
การวิจัยที่เกี่ยวข้องกับมนุษย์ (จำนวน 13 ชุด)
2.1 การเปลี่ยนแปลงโครงร่างวิจัย (ดำเนินการก่อนหนังสือรับรองหมดอายุ ล่วงหน้า 2 เดือน)
การวิจัยที่ไม่เกี่ยวข้องกับมนุษย์ (จำนวน 10 ชุด)
2.1 การเปลี่ยนแปลงโครงร่างวิจัย (ดำเนินการก่อนหนังสือรับรองหมดอายุ ล่วงหน้า 2 เดือน)
- ♦ บางโครงการอาจได้รับการตรวจเยี่ยม (Inspection) จากคณะกรรมการฯ ตามเงื่อนไขที่กำหนดระหว่างการดำเนินการวิจัย
- ♦ คลินิกจริยธรรมการวิจัย (ผู้วิจัยสามารถประสานขอวัน หรือนัดหมายผ่านทางสำนักงานเลขานุการฯ)
- สำนักงานเลขานุการคณะกรรมการจริยธรรมการวิจัย
- กรมควบคุมโรค กองนวัตกรรมและวิจัย
- อาคาร 10 ชั้น 1 ถนนติวานนท์ ต.ตลาดขวัญ อ.เมือง จ.นนทบุรี 11000
- โทรศัพท์ 02-5903149, 062-553-0068
- E-mail: [email protected]
- ฝ่ายเลขานุการ คณะกรรมการจริยธรรมการวิจัย กรมควบคุมโรค
- นางสาวอรวี ลี้เกษร
- นางสาวสุนิสา ปานสอาด
- นางสาวกัญญาณัฐ บุญเข็ม
- นางสาวสุรัสวดี กลิ่นชั้น

